Agostino Di Ciaula;2017
法尼醇X受體(FXR):FXR是核受體家族成員,主要參與膽汁酸代謝和脂質調節。
維甲酸X受體(RXR):類視黃醇X受體,可與多種配體結合,激活后影響特定基因的轉錄,進而對細胞的生長、分化以及脂質、糖代謝等發揮重要的調控作用,比如在脂肪細胞分化、血脂調節等諸多方面都起著關鍵作用。
小異二聚體伴侶(SHP):SHP是一種孤兒核受體,通過與其他受體(如LRH-1)形成異二聚體發揮抑制作用。
肝臟受體同源物-1(LRH-1):屬于核受體超家族,與類固醇生成因子1(SF-1)高度同源。
肝臟X受體(LXR):LXR主要參與膽固醇代謝和炎癥反應調控。
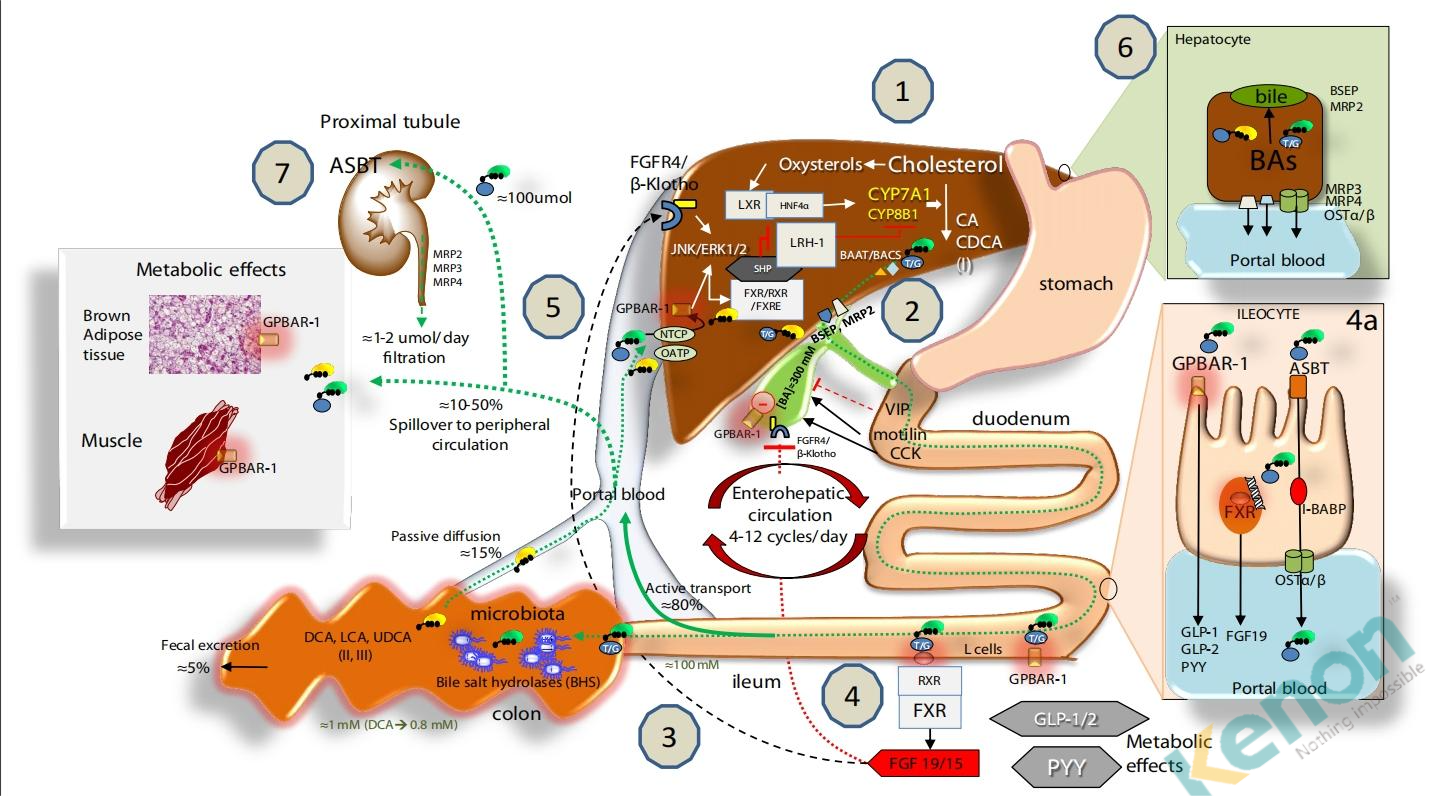
1.在肝臟中,BAs主要由膽固醇通過限速酶7α-羥化酶(CYP7A1)和CYP8B1經“經典途徑”合成,以及通過CYP27A1經“替代途徑”合成。BA主要通過兩種酶與牛磺酸或甘氨酸結合,這兩種酶是BA輔酶A合成酶(BACS)和BA輔酶A-氨基酸N-乙酰轉移酶(BAAT),它們由膽鹽外排泵(BSEP)分泌到膽汁中;多藥耐藥相關蛋白(MRP2)介導有機底物如膽紅素和谷胱甘肽的分泌。
2.在膽囊中,由于水分吸收,膽汁被濃縮和儲存,在進食之后由于腸激素膽囊收縮素CCK8的作用定期釋放到十二指腸。這種節律活動還與膽囊放松/再充盈同步調節,這歸因于血管腸肽(VIP,由胃酸在十二指腸釋放)、膽汁酸本身(作用于膽囊受體GPBAR-1)以及腸道FGF15/19(在回腸中膽汁酸與FXR相互作用后)對FGF4/β-Klotho受體的作用,該受體也在膽囊中表達。健康受試者的空腹血清膽汁酸濃度為0.2-0.7μM,在每餐后增加到4-5μM。
3.膽汁酸在回腸末端被高效(>95%)重吸收。膽汁酸進入結腸,經腸道微生物群生物轉化生成次級膽汁酸,并通過被動擴散和重吸收過程。每天只有5%的膽汁酸以糞便形式排出體外。膽汁酸的肝腸循環包括其在腸道中的重吸收以及通過門靜脈持續回流至肝臟的過程。大約10-50%的重吸收膽汁酸會溢出到外周系統循環中。
4.到達回腸后,膽汁酸激活FXR并增加腸激酶纖維母細胞生長因子19(人類為FGF19或小鼠為FGF15)的轉錄,該因子進入門靜脈循環,調節膽囊(2)和肝臟效應(5)。腸道中的膽汁酸還激活G蛋白偶聯受體(GPBAR-1),刺激肽YY(PYY)、胰高血糖素樣肽1(GLP-1)和胰高血糖素樣肽2(GLP-2)的分泌,這些物質對葡萄糖代謝、胰島素代謝和食欲產生重要影響,作用于位于棕色脂肪組織和肌肉細胞中的GPBAR-1受體。在回腸細胞中,膽汁酸的攝取、胞內運輸和分泌到門靜脈分別需要頂端鈉依賴性膽汁酸轉運蛋白(ASBT)、細胞內膽汁酸結合蛋白(I-BABP)和基底外側異二聚有機溶質轉運蛋白(OSTα/β)(4a)。
5.循環中的FGF19與肝臟FGF受體4(FGFR4)/β-結節蛋白結合,激活c-Jun氨基末端激酶/細胞外信號調節激酶(JNK/ERK)信號通路,該通路協同FXR-SHP抑制途徑,抑制CYP7A1和CYP8B1的表達及肝臟BA合成。肝臟通過鈉膽酸共轉運多肽(NTCP)和有機陰離子轉運多肽(OATP)轉運蛋白進入肝臟,作為生理核配體與FXR結合,通過與RXRs形成異二聚體來調控靶基因轉錄。這導致小異二聚體伴侶(SHP)表達的轉錄增加。SHP繼而抑制LRH-1,阻止參與膽汁酸和脂肪酸合成的目標基因被激活。在沒有膽汁酸的情況下,LRH-1與LXR共同作用,刺激膽汁酸的合成。FXR還調節參與膽汁酸與甘氨酸或牛磺酸結合以及肝臟膽汁酸分泌的酶活性,包括BSEP和ABCB4介導的肝磷脂分泌。重新進入肝臟的膽汁酸還會與庫普弗細胞中表達的肝GPBAR-1相互作用,協同FGFR4/β-Klotho激活的途徑。FXR的激活還協調膽汁酸解毒酶(如胞質硫酸轉移酶2A1 [SULT2A1]、醛酮還原酶1 B7 [AKR1B7]、細胞色素P450 3A4/3a11 [CYP3A4/ Cyp3a11]和UDP-糖基轉移酶2B4 [UTG2B4])的活性。
6.膽汁酸從肝細胞排入門靜脈的過程:特定轉運蛋白包括多藥耐藥蛋白3和4(MRP3、MRP4)以及OSTα/β。
7.從外周循環中,BAs還通過近端小管頂端鈉依賴性膽汁酸轉運蛋白(ASBT)進入腎臟。BAs的腎小球濾過受MRP2、3、4轉運蛋白的調節。